Africa-Press – Guinee Bissau. Si la recherche contre la maladie de Parkinson avance rapidement, grâce à de nouveaux traitements qui améliorent la qualité de vie des patients, ils s’attaquent seulement aux symptômes sans véritablement ralentir la neurodégénérescence à l’origine de la maladie. « Trouver un traitement qui protège réellement les neurones est le graal des neurosciences « , lance le professeur John Mitrofanis, spécialiste des maladies neurodégénératives à Clinatec (Grenoble) et à l’université de Sydney (Australie). Or, avec son équipe, ce chercheur australien pourrait justement avoir trouvé ce graal. Un traitement qui promet d’augmenter la survie des neurones et de ralentir la progression de la maladie: la lumière.
La maladie de Parkinson est caractérisée par un déficit de dopamine, causé par la perte progressive des cellules qui produisent ce neurotransmetteur, les neurones dopaminergiques. Or, les lumières rouge et proche infrarouge parviennent à stimuler le métabolisme de ces neurones, les protégeant de la neurodégénérescence. « Grâce à la lumière, ils survivent plus longtemps, autant chez la souris malade que chez des primates non humains, résume John Mitrofanis. Chez ces derniers, qui ont des signes cliniques très similaires à ceux observés chez l’humain atteint de Parkinson, nous observons également une amélioration des symptômes. » Ces études pré-cliniques, publiées entre 2014 et 2017, ont ouvert la voie au premier essai clinique chez l’humain, encore en cours.
Les bienfaits de la lumière théorisés depuis les années 1960
Pourtant, cette technique novatrice… n’est en réalité pas si neuve. Les bienfaits de la lumière sont théorisés depuis l’Égypte ancienne, mais ce n’est que dans les années 1960 qu’a été trouvée une façon de l’utiliser de manière focalisée pour soigner une partie du corps. Le pionnier est Endre Mester, chirurgien hongrois qui utilisa pour la première fois un laser de basse intensité pour réduire l’inflammation de la peau. Depuis, cette méthode, connue comme photobiomodulation, est employée notamment par des physiothérapeutes et dans des médecines alternatives.
Mais ce n’est que depuis une dizaine d’années que des preuves scientifiques ont validé son bien-fondé, créant un intérêt dans le monde de la recherche en neurosciences. « La lumière du soleil est composée de plusieurs longueurs d’onde qui varient durant la journée: le matin, la lumière bleue est majoritaire, et cela nous aide à nous réveiller et à nous focaliser ; le soir, le rouge et l’infrarouge prennent le dessus et sont censés aider notre corps à se réparer, explique John Mitrofanis. Nous appliquons au cerveau cette dernière partie du spectre lumineux. »
Mais pourquoi cette lumière est-elle bénéfique pour le corps? Des études récentes montrent que la lumière proche de l’infrarouge agit directement sur les usines énergétiques des cellules, les mitochondries, en augmentant leur production d’énergie. « Il y a probablement aussi une action anti-inflammatoire et une modification de l’expression de certains gènes qui interviennent dans les processus de ralentissement du vieillissement cellulaire « , ajoute Stephan Chabardès, chef du service neurochirurgie au CHU Grenoble Alpes et responsable du secteur hospitalier de Clinatec. Avec son équipe, il cherche à savoir si ces effets sur la cellule permettent de protéger les neurones dopaminergiques, responsables de la sécrétion de dopamine dans la substance noire (structure à la base du cerveau qui participe au contrôle de la motricité), et qui succombent petit à petit dans la maladie de Parkinson.
La lumière à l’origine de la vie?
Pourquoi des cellules enfouies dans l’obscurité du cerveau sont-elles encore sensibles à la lumière? Pour l’expliquer, John Mitrofanis, spécialiste des maladies neurodégénératives à Clinatec (Grenoble), avance deux hypothèses. D’abord, il s’agirait d’un vestige de nos ancêtres unicellulaires, chez qui la lumière du soleil aurait joué un rôle important. En devenant de plus en plus complexes, les organismes auraient simplement gardé cette capacité, même dans les cellules désormais cachées de la lumière.
Mais il se pourrait aussi que les cellules aient retenu ce lien avec la lumière volontairement: « Les cellules ne font pas que recevoir, elles émettent aussi de la lumière sous la forme de biophotons, révèle-t-il. Et cette émission change en fonction de l’état de la cellule. » Il se pourrait donc qu’elles s’en servent aussi comme système de communication cellulaire, pour dire aux voisines si elles vont bien ou pas. Une possibilité actuellement à l’étude.
Dans l’expérience, la lumière est émise directement à l’intérieur du cerveau, grâce à un dispositif implantable similaire à celui utilisé pour la stimulation cérébrale profonde (qui sert à traiter les symptômes de la maladie de Parkinson avec de l’électricité). Elle est délivrée à l’intérieur de la boîte crânienne à travers une fibre optique, dans des longueurs d’onde allant de 600 à 1300 nanomètres, afin de stimuler les neurones.
Cet essai clinique de phase 1 (dite de sécurité car le but principal est de montrer que la technique est sûre) compte 14 patients, diagnostiqués il y a moins de deux ans. Sept ont reçu la sonde lumineuse et sept une sonde factice pour quatre ans. Le dernier patient a été opéré en octobre dernier. En janvier 2025, Stephan Chabardès a présenté dans un préprint (des travaux qui n’ont pas encore été validés par les pairs) les résultats préliminaires sur deux ans de traitement pour les trois premiers patients inclus dans l’étude, avec des résultats très encourageants. « L’implantation de cette sonde se passe bien et l’illumination infrarouge en continu est bien tolérée, il n’y a pas d’effets secondaires graves « , résume le chercheur.
Les capacités motrices des patients, évaluées tous les six mois, montraient une légère amélioration alors que les patients non traités présentaient une forte dégradation. Cette diminution des symptômes était observée aussi dans leur démarche, qui ne ralentissait pas comme chez les patients non traités.
Intervenir au début de la maladie
Des analyses d’imagerie cérébrale ont révélé que les cerveaux des patients traités produisaient davantage de dopamine un an après le début du traitement, montrant que la lumière stimulait bien les neurones dopaminergiques, ce qui expliquerait l’atténuation des symptômes. « On a l’impression que leur maladie évolue moins vite, s’enthousiasme Stephan Chabardès, tout en restant prudent: attendons les résultats à deux ans de tous les malades et espérons qu’ils confirmeront ces premières observations. »
Si c’est le cas, la prochaine étape sera de faire une étude avec un plus grand nombre de patients, dans le but de les traiter dans les étapes précoces de la maladie de Parkinson. Cependant, même si son efficacité est confirmée, il ne s’agira pas pour autant d’un traitement miracle: « On ne va pas guérir la maladie ; les patients auront toujours besoin de médicaments, peut-être même de la stimulation cérébrale profonde, précise-t-il. Ce qu’on essaie, c’est de faire en sorte d’améliorer l’évolution de la maladie en ralentissant le processus de dégénérescence. »
Le bémol, c’est que pour être efficace, cette technique devra être appliquée au début de la maladie. Puisque le but est de protéger les neurones dopaminergiques, il faudra intervenir au moment où il y a encore un bon nombre de ces cellules dans la substance noire, avant qu’elles ne soient emportées par la neurodégénérescence. Le patient devra ainsi prendre la décision de subir une chirurgie invasive du cerveau (pour implanter la sonde), avec les risques que cela peut comporter, à un moment de la maladie où les symptômes ne sont pas encore très prononcés et où les traitements traditionnels sont encore efficaces pour les atténuer. « Oui, c’est une approche invasive, mais les risques sont mesurés, rassure Stephan Chabardès. Et il faut insister sur le fait que seule la photobiomodulation pourrait retarder la progression de la maladie, ce que les autres traitements ne permettent pas. » Sa conclusion: le rapport risque-bénéfice serait largement favorable.
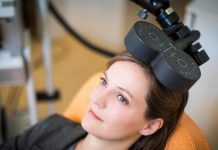
Ce rapport serait meilleur encore pour d’autres utilisations possibles de cette technologie. C’est notamment le cas de la maladie d’Alzheimer: les parties du cerveau affectées étant bien plus proches de la surface – principalement au niveau du cortex -, elles peuvent être stimulées de manière non invasive. Pour ce faire, la start-up montpelliéraine Regenlife a conçu un dispositif qui lui a valu une nomination au prix Galien USA 2025: un casque modulaire qui s’ajuste à la morphologie crânienne de chacun… et à sa chevelure: « Les cheveux reflètent beaucoup de lumière, peu d’ondes lumineuses sont à même de les traverser, explique Guillaume Blivet, fondateur de la start-up. Les composants optiques de notre casque sont reliés à un guide qui va traverser les cheveux comme un peigne pour se poser directement sur le cuir chevelu. »
La technique pourrait être utilisée pour les infarctus
L’entreprise a une autre cible: le microbiote intestinal, afin d’agir sur l’ensemble de l’axe cerveau-intestin grâce à une ceinture abdominale. « L’existence d’une communication bidirectionnelle entre le cerveau et l’intestin est de plus en plus documentée, notamment pour les maladies neurodégénératives, rappelle-t-il. Nous avons mis en évidence que la photobiomodulation donne de meilleurs résultats quand elle est appliquée en double [cerveau-intestin] plutôt qu’avec une simple application sur le cerveau. » Le dispositif est à l’étude dans un essai clinique de phase 3 en collaboration avec le CHU de Toulouse et l’Assistance publique-hôpitaux de Paris (AP-HP). Une centaine de patients y sont traités durant six mois, avec un suivi de la même durée après l’arrêt du traitement. L’essai devrait rendre ses conclusions dans un an, et, si les résultats sont positifs, Guillaume Blivet espère une mise sur le marché fin 2027.
En dehors des maladies de Parkinson et d’Alzheimer, la photobiomodulation pourrait être utilisée pour un très grand nombre de pathologies. En effet, les mitochondries qu’elle stimule sont présentes dans toutes les cellules du corps ! Elle est ainsi expérimentée pour traiter la maladie à corps de Lewy (maladie neurodégénérative qui cause des troubles cognitifs et des hallucinations), les traumatismes crâniens, les troubles du sommeil et les infarctus. « Nous avons développé un dispositif en forme de gilet, qui peut être utilisé le plus tôt possible après un infarctus du myocarde dans le but de limiter la propagation de la mort des cardiomyocytes et ainsi éviter l’évolution vers l’insuffisance cardiaque, fréquente chez les patients « , affirme Laurent Hérault, directeur du fonds de dotation Clinatec, où cette étude est menée.
Le traitement par la lumière serait-il en passe de bousculer la médecine durablement? « Cette technologie a énormément d’avantages: elle a un coût accessible et elle peut être déployée à grande échelle « , martèle Guillaume Blivet. Néanmoins, le chemin est long car, dans les esprits, elle reste associée aux médecines alternatives. « Je n’y ai pas cru la première fois que j’en ai entendu parler, il y a une vingtaine d’années, avoue John Mitrofanis. Il a fallu que je le voie de mes propres yeux, expérimentalement. Je pense que les gens commencent à accepter le bien-fondé de cette approche, mais une grande partie de la communauté médicale ne croit pas encore que la lumière puisse avoir une influence sur la fonction cellulaire, au moins au point d’être thérapeutique. » Ces essais cliniques pourraient les éclairer.
Illuminer les mitochondries pour protéger la cellule
Au sein des mitochondries, l’énergie est produite dans la chaîne respiratoire: un ensemble de complexes protéiques utilise l’oxygène pour produire de l’ATP, la molécule énergétique des cellules. La lumière proche de l’infrarouge a un effet direct sur ce processus, car elle est captée par une de ses protéines clés, l’oxydase de cytochrome c. Cela stimule son fonctionnement, augmentant le rendement de la chaîne respiratoire, et donc la production d’ATP. Cette optimisation mitochondriale a aussi comme conséquence une diminution du stress oxydatif, produit en excès lorsque cette organelle est dysfonctionnelle. Ainsi, la lumière a un effet double très rapide: les cellules ont plus d’énergie et elles sont protégées du stress.
« Les mitochondries sont essentielles pour la cellule, car elles produisent l’énergie utilisée dans une grande partie des processus cellulaires, rappelle John Mitrofanis, spécialiste des maladies neurodégénératives à Clinatec (Grenoble). Quand la mitochondrie va mal, la cellule va mal… et inversement, quand la mitochondrie fonctionne bien, la cellule aussi se porte mieux. » Et ces bénéfices ne s’arrêtent pas à la mitochondrie, car celle-ci communique constamment avec le noyau cellulaire, où réside le génome. Grâce à cette amélioration de la fonction mitochondriale, les signaux envoyés au noyau changent aussi, activant l’expression d’une vingtaine de gènes qui stimulent la cellule et la protègent. Cette modification de la transcription génétique a des effets sur le long terme, qui sont visibles des semaines, voire des mois après la stimulation lumineuse. « On a donc des effets à court et à long termes qui améliorent la survie cellulaire, surtout lorsque les cellules sont sous un stress, résume le chercheur. C’est extrêmement efficace, et, en théorie, cela pourrait fonctionner avec tout type de cellule. »
Pour plus d’informations et d’analyses sur la Guinee Bissau, suivez Africa-Press