Africa-Press – Guinee Equatoriale. En 1865, Louis Pasteur est appelé à la rescousse. Le dépérissement des vers à soie met en péril la filière cévenole. C’est grâce à son microscope qu’il découvre le parasite responsable de la maladie, la pébrine, mais aussi qu’il élabore une méthode permettant de séparer les œufs atteints des œufs sains. Le microscope lui permet d’observer ce qui n’est pas visible à l’œil nu en changeant d’échelle, de comprendre son organisation, et même de pouvoir agir. Aujourd’hui encore, on continue de repousser les frontières du visible avec l’accès à des détails de plus en plus précis : au-delà de la morphologie, on devient capable, grâce à la microscopie de super-résolution, d’observer le vivant en train de fonctionner.
Cette capacité de plonger à l’intérieur d’un tissu a toujours stimulé les questionnements des biologistes et été à l’origine de nouvelles hypothèses. N’est-ce pas grâce à l’imagerie que Santiago Ramón y Cajal peut affirmer, dès la fin du 19e siècle, que le cerveau n’est pas une masse gélatineuse – ce qu’on croyait jusqu’alors – mais qu’il est constitué de cellules individuelles ? N’est-ce pas encore l’imagerie qui, aujourd’hui, permet de visualiser des virus en 3D et de trouver des cibles accessibles à de nouveaux médicaments ?
L’imagerie est devenue une discipline à part entière, avec sa propre communauté de scientifiques dont les recherches ont pour objet… l’imagerie. Enfin, autre évolution de ces vingt dernières années, les instruments, aussi perfectionnés qu’onéreux, sont regroupés et mutualisés sur des plateformes où biologistes, généticiens et neuroscientifiques réalisent leurs expériences avec l’aide de spécialistes en imagerie. Assez loin de l’image… du scientifique seul devant sa paillasse.
La microscopie optique, pour en voir de toutes les couleurs
L’utilisation des premiers microscopes optiques remonte à la fin du 16e siècle. Encore aujourd’hui, ces microscopes, aussi appelés photoniques, restent indispensables aux chercheurs. Ils reposent sur le même principe : il s’agit d’agrandir l’image d’un échantillon, traversé par de la lumière (les photons), grâce à des lentilles. Ceci nécessite la plupart du temps de colorer les tissus afin de distinguer clairement les détails. Pour les cellules eucaryotes, par exemple, on utilise l’éosine pour colorer le noyau en violet et le cytoplasme en rose. Il existe aussi des colorations spécifiques aux cellules que l’on souhaite mettre en évidence dans l’échantillon : la coloration de Gram permet de visualiser les bactéries, celle de Golgi les neurones, etc.
Née dans les années 1980, la microscopie de fluorescence repose, elle, sur des marqueurs fluorescents grâce auxquels on peut cibler spécifiquement une protéine ou encore un lipide. La microscopie à super-résolution permet quant à elle de dépasser la limite de la microscopie optique traditionnelle, 200 nanomètres. Avec cette technique, on atteint une résolution de l’ordre de la dizaine de nanomètres, et donc un changement d’échelle dans la compréhension du vivant.
Exemple largement utilisé en neurobiologie, le marquage des ions calcium par fluorescence permet de suivre leur libération lors du passage d’un influx nerveux et de repérer les neurones activés. À la différence de la microscopie électronique, la microscopie optique permet de travailler sur des éléments vivants et de visualiser en temps réel des mécanismes tels que l’invasion d’un tissu par une bactérie.
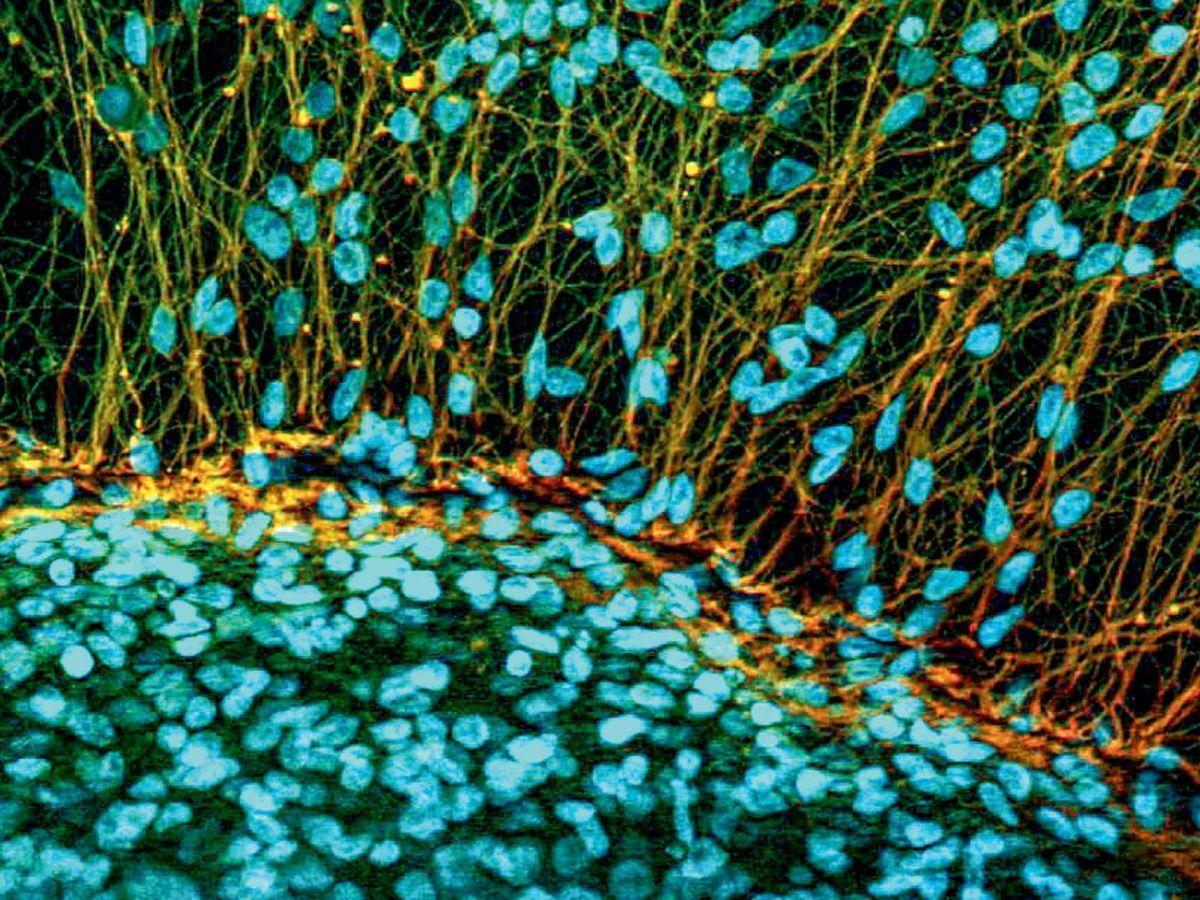
COLORATION DE GOLGI
À la fin du 19e siècle, le médecin italien Camillo Golgi met au point une technique de coloration des cellules nerveuses reposant sur l’utilisation du nitrate d’argent, qui permet de les visualiser au microscope photonique. Ce marquage, grâce auquel on obtint pour la première fois des images morphologiques très précises des cellules et de la complexité des réseaux neuronaux, est encore utilisé aujourd’hui. Outre la morphologie des neurones, cette coloration permet d’estimer la densité des circuits nerveux car, sans qu’on comprenne pourquoi, seul un neurone sur mille est marqué.
FLUORESCENCE
Les fluorophores sont des molécules qui émettent de la fluorescence en réponse à une excitation par un faisceau de photons. Les chercheurs s’appuient sur des molécules qui ont cette propriété naturelle, ou marquent avec un fluorophore la molécule qui les intéresse si elle en est dépourvue. Dans cette photo d’un œil de poisson-zèbre (ci-dessous), animal modèle en biologie, les vaisseaux sanguins sont visibles en rouge et les vaisseaux lymphatiques en bleu.
Vers l’infiniment petit…
Inventé dans les années 1930, le microscope électronique ressemble à un microscope optique, mais la source d’illumination de l’échantillon est un faisceau d’électrons accélérés sous vide dans des tubes cathodiques. Comme la longueur d’onde du faisceau électronique est plus courte que celle d’un rayon photonique, la résolution est meilleure. Fixés en général dans la résine, les coupes ultrafines des échantillons à étudier peuvent être aussi figées dans le froid. Développée à partir des années 1980, la cryomicroscopie électronique présente l’avantage de préserver la structure de l’échantillon et d’éviter les déformations. La microscopie électronique permet donc d’observer à une échelle très petite, de l’ordre de l’atome, avec une fidélité à la réalité presque parfaite.
ZOOM SUR LES VIRUS
La microscopie électronique à transmission est la technique d’imagerie privilégiée pour visualiser les virus, compte tenu de leur petite taille. Le virus de la grippe, par exemple, mesure environ 100 nanomètres. Ci-dessous, des particules du virus de la grippe souche porcine SW31.
Fusionner les images
Les chercheurs utilisent souvent plusieurs types de microscopes pour obtenir des vues d’ensemble, puis des détails. Différents échantillons sont nécessaires car le traitement réalisé pour l’imagerie (colorant, fluorochrome, résine…) abîme l’échantillon, qui n’est donc pas utilisable plusieurs fois. Un des enjeux actuels est d’être capable de regarder un même échantillon biologique en microscopie photonique puis en microscopie électronique. Il s’agit de la microscopie corrélative ou Clem (pour “Correlative Light and Electron Microscopy”) : par exemple, elle permet de visualiser des protéines de la membrane des neurones actives au passage de l’influx nerveux grâce à un marquage fluorescent, la synapse étant figée par le froid afin d’être visualisée en détail par cryomicroscopie électronique.
POINTS DE REPÈRE
Pour s’assurer qu’ils observent la même région d’un échantillon lorsqu’ils font appel à des techniques différentes, les chercheurs se repèrent à l’aide d’un marquage, qui doit être commun. Par exemple, des billes fluorescentes qui peuvent aussi être des repères révélés par des électrons. Sur ces cellules de peau, les points en fluorescence rouge visibles en microscopie optique correspondent à des billes noires visibles en microscopie électronique. Il est possible de superposer les deux images.
Pour plus d’informations et d’analyses sur la Guinee Equatoriale, suivez Africa-Press