Africa-Press – Benin. Dans un bloc opératoire du CHU de Toulouse, une abdominoplastie touche à sa fin. L’excès de peau qui vient d’être retiré du patient est soigneusement mis de côté. D’ordinaire voué à la destruction, ce morceau de peau va être collecté pour devenir, dans quelques heures, un outil précieux pour la recherche. La peau est récupérée par des transporteurs spécialisés puis arrive sous 24 heures maximum après la chirurgie dans les laboratoires de Genoskin, une biotech spécialisée dans le recyclage d’échantillons de peau.
Réceptionnée au centre Pierre-Potier de Toulouse, une pépinière d’entreprises innovantes où est installée Genoskin depuis 2011, cette peau, composée de l’épiderme, du derme et de l’hypoderme, est prise en charge par une équipe de production. Elle est dégraissée, biopsiée, désinfectée puis mise en culture, afin de devenir un modèle fonctionnel qui permettra de tester l’efficacité et la tolérance des traitements médicaux, comme des anticorps monoclonaux injectables.
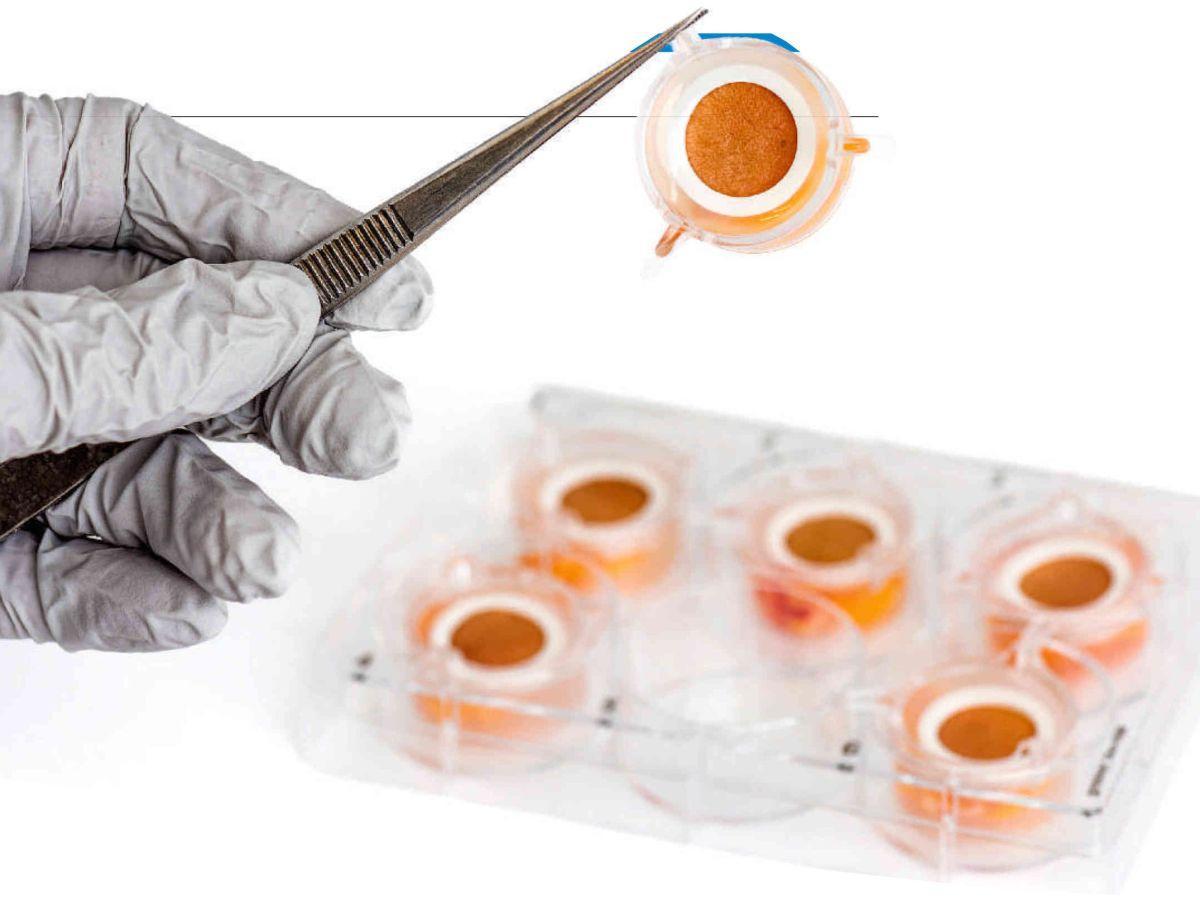
« Nous avons créé un gel qui vient emprisonner la biopsie de peau et permet de laisser sa surface au contact de l’air. Cela permet aussi de faire une tension mécanique pour ne pas que le morceau de peau se referme sur lui-même », explique Pascal Descargues, P-DG de Genoskin. C’est lors de son post-doctorat à l’université de Californie à San Diego (États-Unis) que ce dernier, alors chercheur en maladie génétique de la peau, prend conscience des limites éthiques et scientifiques des modèles animaux. Il se tourne alors vers une matière jusque-là négligée: les déchets chirurgicaux issus d’opérations d’abdominoplasties, en pleine expansion avec l’épidémie mondiale d’obésité.
La peau prélevée reste « vivante » pendant sept jours
L’innovation de l’entreprise réside dans un milieu de culture qui permet de nourrir le tissu et de préserver les cellules. Grâce à cette technologie brevetée exclusive en France, la peau est gardée vivante pendant sept jours et les caractéristiques immunologiques du donneur sont conservées. « Pour que les organes et tissus humains soient réellement utiles en recherche, ils doivent rester vivants: ni congelés, ni conservés au réfrigérateur. Comme nous, ils vivent à 37 °C », précise Pascal Descargues.
Les matrices sont ensuite proposées aux clients de Genoskin sous forme de kits, prêts à l’emploi. Certains sont composés de l’épiderme et du derme, d’autres incluent l’hypoderme. Chaque kit est accompagné d’informations précises sur le donneur: âge, sexe, type de peau et site anatomique. « Il y a un cadre réglementaire très strict. Nous rémunérons les hôpitaux non pas pour les échantillons de peau fournis, mais pour le temps passé à les obtenir. C’est une compensation financière minime qui est uniquement associée au dédommagement de la prestation », précise Benoît Lavabre, responsable de la biobanque de Genoskin. Le client, lui, n’achète pas la peau mais la matrice qui va avec, en fonction de ses critères spécifiques: « Nous connaissons les plannings opératoires à l’avance et nous nous positionnons en fonction des critères de sélection des études. Par exemple, nous pouvons avoir besoin d’un phototype particulier, d’un certain âge ou d’un sexe spécifique. Cela nous permet de répondre à des critères d’inclusion très précis et très sélectifs. »
Pour autant, la solution proposée connaît encore certaines limites. « Il manque un composant qui est jugé essentiel dans de plus en plus de maladies, c’est le système nerveux périphérique, explique Vincent Flacher, directeur de recherche à l’Institut de biologie moléculaire et cellulaire (IBMC) du CNRS. Lorsqu’un chirurgien prépare cette pièce de peau, les axones des neurones sensoriels sont coupés, et ce qu’il reste, ce sont des fragments qui ne vont plus remplir leurs fonctions. » Cela pose problème, notamment pour des maladies comme le psoriasis ou la dermatite atopique, où les neurones peuvent influencer l’inflammation cutanée: « Les neurones ne sont probablement pas à l’origine de ces maladies, concède le chercheur, mais il pourrait y avoir des interactions entre le système immunitaire et le système nerveux qui régulent l’inflammation et pourraient l’exacerber. » Pour Vincent Flacher, le futur de la recherche réside donc dans « la construction de modèles 3D innervés ou la réinnervation in vitro des explants ».
Des clients dans l’industrie pharmaceutique et cosmétique
C’est justement le travail mené par Nicolas Lebonvallet, ingénieur de recherche au laboratoire Interaction épithéliums neurones de l’université de Bretagne occidentale, qui a mis au point avec son équipe, et après quinze années de recherche, un modèle unique de peau réinnervé par des neurones humains.
« Nous avons réussi à réintroduire des neurones sensoriels humains, issus de cellules souches de la peau provenant de déchets opératoires, dans un explant de peau », explique le chercheur. L’objectif scientifique de ce modèle est de comprendre les interactions neurocutanées: non seulement la sensorialité, mais aussi les apports des neurones à la physiologie de la peau. Et, inversement, d’observer comment le tissu cutané contribue à l’innervation et à la composante sensorielle. » Un modèle de peau désormais commercialisé par le laboratoire Bio-EC, pour des tests cosmétiques et pharmaceutiques.
Genoskin compte parmi ses clients de grands noms de l’industrie pharmaceutique (Sanofi, AstraZeneca), de la grande consommation (Colgate, Unilever) et des cosmétiques (L’Oréal, Estée Lauder, Yves Rocher, Shiseido). Ces derniers y ont recours pour tester les réponses immunitaires et les effets secondaires de leurs produits, bien avant les essais cliniques sur l’humain. Un gain de temps et d’argent précieux: « Le développement d’un médicament prend entre 10 et 15 ans, coûte de 1 à 2 milliards d’euros et 90 % des projets sont en échec. Neuf molécules sur dix n’iront jamais sur le marché », argumente Pascal Descargues. Genoskin se décrit comme une « gare de tri », capable de sélectionner les projets qui apportent les meilleurs résultats et d’éliminer ceux qui se révéleront toxiques pour l’humain. L’objectif est d’apporter des données fiables pour un développement de médicaments plus prédictif, mais aussi plus éthique.
L’entreprise a ainsi développé un vaste réseau de collecte de peau humaine avec des hôpitaux, des cliniques, ainsi que des biobanques et des laboratoires privés: « Nous travaillons avec 17 sites aux États-Unis et 12 en France. Cela représente aujourd’hui un accès à plus de 2000 donneurs par an. » De fait, Genoskin a profité d’un marché en plein essor, porté par l’évolution de la réglementation: depuis 2013, l’Union européenne interdit la vente de produits cosmétiques testés sur les animaux. L’Inde a suivi en 2014 comme plusieurs États américains, notamment la Californie. C’est dans ce contexte que d’autres acteurs se sont développés pour répondre à une demande croissante de modèles cutanés humains. C’est le cas de la société lyonnaise CTI Biotech, spécialisée dans le développement de peau humaine en impression 3D, ou de l’écossais TenBio, qui travaille comme Genoskin sur de la peau humaine native ex vivo. La marque L’Oréal avait, elle, créé Episkin dès 1997, un centre de recherche et d’innovation consacré à la reconstruction de peau humaine à partir de déchets opératoires.
Remplacer les modèles animaux
Si les explants de peau offrent un début de solution pour réduire l’expérimentation animale dans le secteur dermatologique, près de 3000 primates non humains étaient encore utilisés en France en 2022, sur un total de deux millions d’animaux. Mais depuis le Covid-19, les macaques destinés aux essais précliniques, venus principalement de Chine, se font rares, et leur coût a explosé: il est passé de 5000 à 30.000 euros l’unité. Le macaque est ainsi devenu un élément géostratégique, au cœur des rivalités internationales avec un risque majeur: voir l’Europe prendre du retard dans la recherche biomédicale. Pour pallier cette menace, un projet du CNRS prévoit l’extension d’un centre d’élevage près de Marseille, qui ambitionne d’héberger 1800 primates d’ici à 2030.
Une extension aux domaines génomiques et protéomiques
Si, à son lancement, Genoskin testait majoritairement des cosmétiques et des médicaments dermatologiques, aujourd’hui, près de 60 % de ses clients proviennent du secteur biotech et pharmaceutique. « Nous avons amélioré notre système pour lui permettre de subir des injections sous-cutanées ou intradermiques. Cela nous ouvre aujourd’hui aux biothérapies: des vaccins, de l’insuline ou des anticorps monoclonaux « , se félicite Pascal Descargues.
Un repositionnement stratégique pour la biotech, qui propose désormais des tests menés en interne pour ajouter une couche d’analyse avancée: les échantillons permettent d’explorer différents types de données biologiques, grâce à des analyses omiques (gènes, ARN, protéines, métabolites…). Ces données sont ensuite étudiées avec des outils de bio-informatique, combinant méthodes statistiques et intelligence artificielle, afin d’identifier les gènes et les populations cellulaires les plus affectés par un produit ou un traitement. Ambition affichée: transformer le mode de développement des biothérapies et permettre l’administration autonome par injection sous-cutanée. « Nous travaillons notamment avec des sociétés qui développent des dispositifs médicaux, tels que des seringues particulières, des auto-injecteurs, des micropompes ou des outils pour mesurer le glucose pour les personnes diabétiques « , ajoute Pascal Descargues. Des solutions qui présentent un double avantage pour le chercheur: plus confortables pour les patients, mais également moins coûteuses pour la société.
Qu’ils soient in vitro ou ex vivo , la communauté scientifique s’accorde à dire que ces modèles de peau ne pourront pas remplacer les animaux à court terme. Mais ces innovations restent un pari scientifique, économique et éthique gagnant pour Genoskin.
Par Céline Labesque